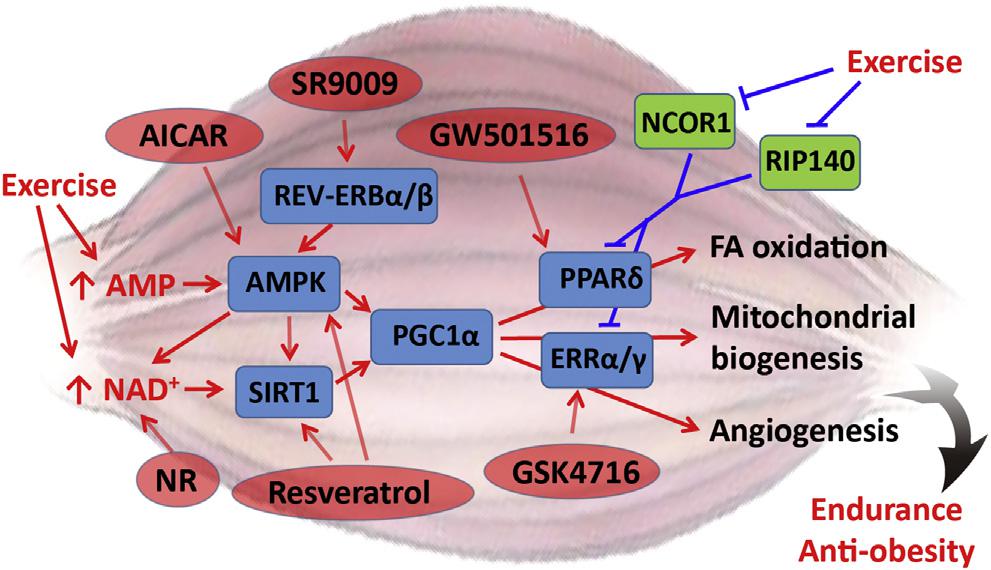
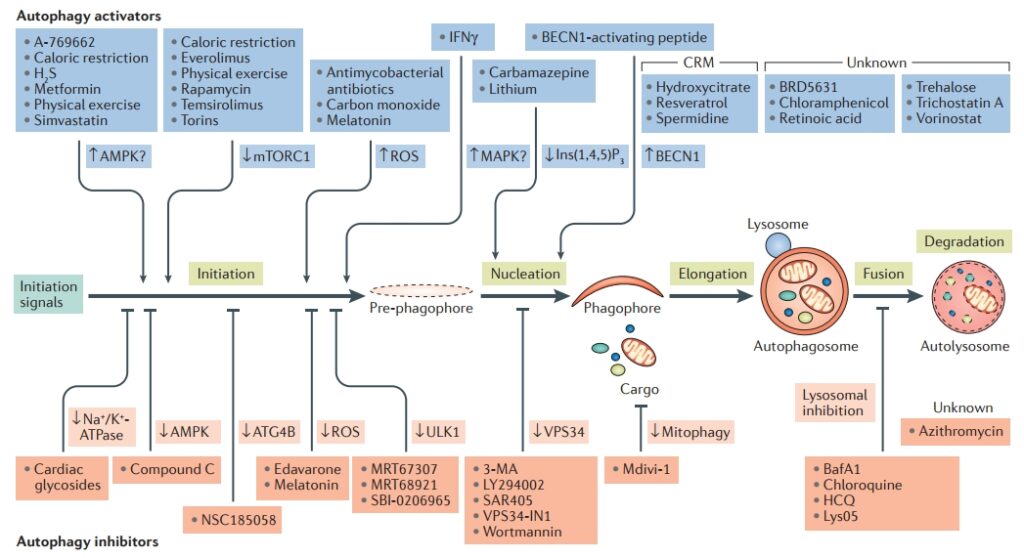
Кверцетин и ресвератрол – комбо, активирующее ось SIRT1 > PGC-1α (окислительный метаболизм, жиросжигание) и AMPK (аутофагия).
Пару недель назад мне пришло в голову совместить это комбо. За неделю я скинул пару килограмм, никак не меняя диету. Затем я нашел, что по этой теме есть исследования. Приятно, что мой мозг начинает работать как надо, может сам складывать 2+2 и выдавать рабочие решения.
Ранее я писал про ось SIRT1 > PGC-1α и про миметики физической нагрузки. Тема миметков физической нагрузки и активации оси SIRT1 > PGC-1α важна не только для “лежачих больных”, но и для людей с ожирением. Интенсивные физические нагрузки для людей с ожирением могут быть не только неполезны, но и крайне вредны. Поиск способов похудания и активации окислительного метаболизма без диеты – важная точка приложения научных усилий. В частности огромный фокус сейчас идет на прекурсорах NAD+.
Меня давно занимать ресвератрол, но в исследованиях его требовалось обычно довольно МНОГО. Например, в этом исследовании ресвератрола на резус-макаках они употребляли 480 мг ресвератрола в день в течение двух лет. При весе в 5-7 кг это 80-100 мг на 1 кг веса. Что 6,4-8 грамм ресвератрола в день для человека весом 80 кг.
Кверцетин также известен тем, что склоняет ткани к оксительному метаболизму.
Кверцетин и ресвератрол. Исследования
Комбо улучшало липидный профиль (↓триглицериды, ↓LDL, ↑HDL, ↓ общий_холестерин) у крыс, у которых диабет был вызван стрептозоцином (токсичное для бета-клеток поджелудочной вещество). При этом различные параметры гомеостаза (в том числе глюкозы были в норме): глюкоза, инсулин, глюкоза-6-фосфат, pH, уровень лактата, anion gap, ферменты печени, креатин, мочевина, супероксид дисмутаза и глутатион. В общем и целом прекрасный результат.
Кроме нормализации веса на фоне комбо кверцетин и ресвератрол, активацией ими сиртуина 1 и AMPK и выше описанных эффектов, тут были иммуннологические тесты. Видим нормализацию ФНОα, IL-6, адипонектина, инсулина итд.
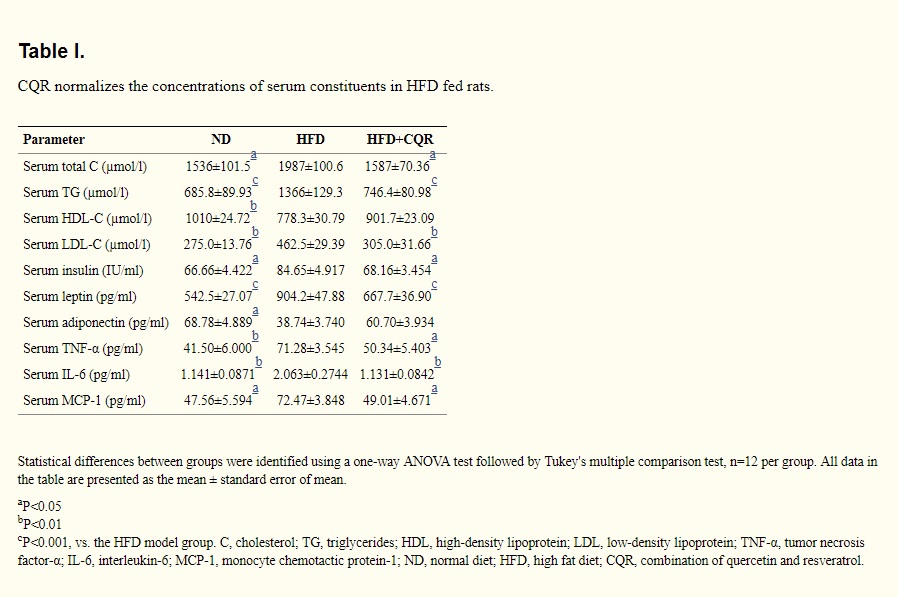
В дополнении к эффекту жиросжигания был интересный эффект, которого не было у этих полифенолов по отдельности. Комбо подавляло ацетил-КоА карбокслазу и тригицерид липазу живой ткани (adipose tissue triglyceride lipase). Ацетил-КоА карбоксилаза катализирует реакцию карбоксилирвоания ацетил-КоА до малонил-КоА – это первая реакция синтеза жиров из ацетил-КоА (который диет в цикл Кребса, а при избытке превращается в жиры). В общем наше комбо подавляет синтез жира,
Кверцетин и ресвератрол. Риски
- Кверцетин подавляет следующие ферменты цитохрома P450: сильное подавление CYP2D6 и умеренное подавление CYP2C19 и CYP3A4;
- Ресвератрол считает сильным ингибиторов CYP1A1.
Перед принятием этого комбо необходимо оценить общее состояние печени и нагруженность искомых ферментов печени лекарствами и ксенобиотиками из диеты.
Кверцетин и ресвератрол, которые употреблял я
- Thorne Research, Quercetin Phytosome, 60 Capsules
- Now Foods, Natural Resveratrol, 200 mg, 60 Veg Capsules
Это месячный курс.
Выводы
- Комбо кверцетин и ресвератрол активирует ось SIRT1 > PGC-1α и AMPK;
- Благодаря этому данное комбо хороший инструмент для улучшение метаболического профиля людей с сахарным диабетом 2-го типа, ожирением, метаболическим синдромом и предиабетом;
- Снижение про-воспалительных цитокинов в том числе накладывающих определнную “ношу” на фукнцию мозга – тоже хорошо (мне очень нравится неточное, но броское определение, что ожирение – воспалительная болезнь мозга);
- Кето и голодание активируют ось NAD+ > SIRT1 > PGC-1α и AMPK; Возможна синтергия кето и вышеупомянутого комбо;
- Так как эти полифенолы подавляют ферменты некоторые P450, надо понимать функцию печени и взвешенно подходить к комбинации курса этих молекул с лекарствами и другими ксенобиотиками.