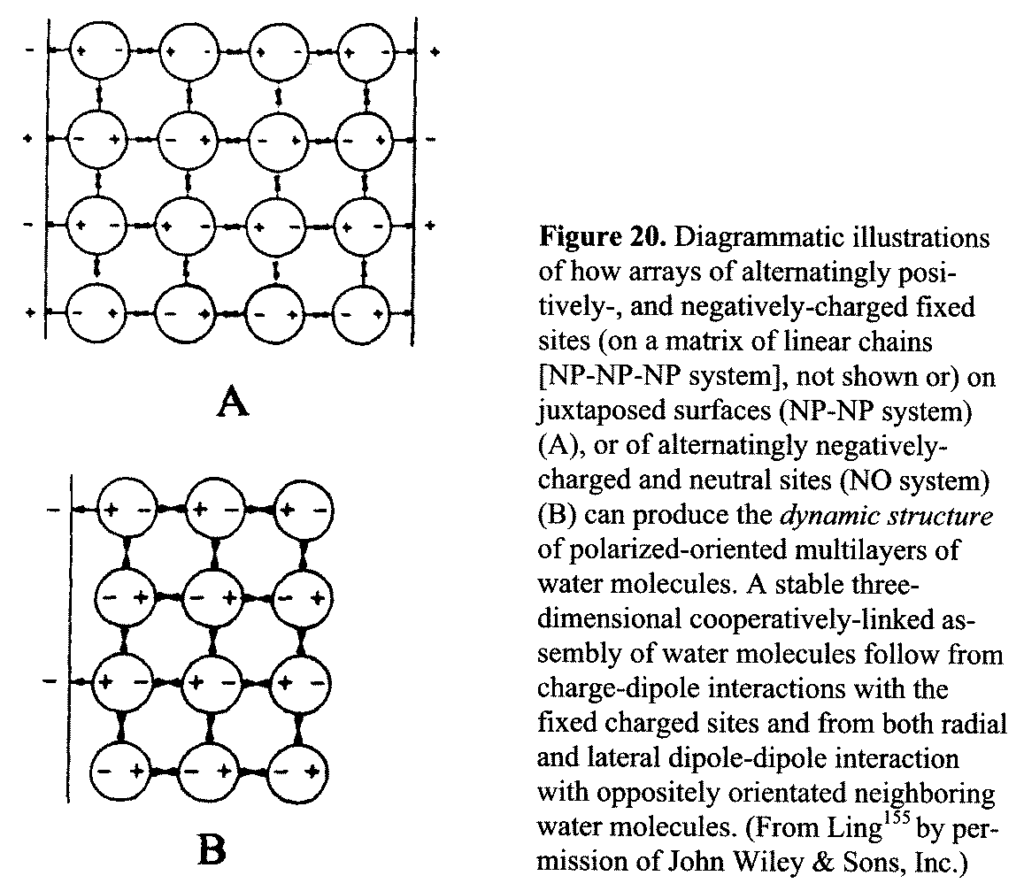
Начну с конца прошлой заметки:
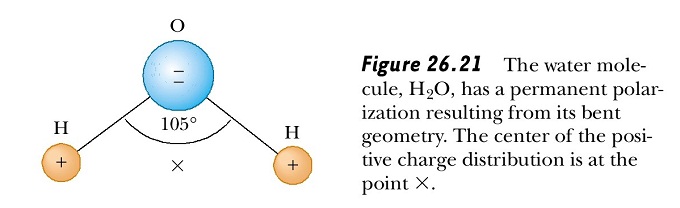
- вода – диполь, обладает дипольным моментом, который увеличивается в присутствии других диполей;
- в полноразвернутой конформации белков CO- (негативные) и NH-группы (положительные) доступны воде и приводят к ее дополнительной поляризации;
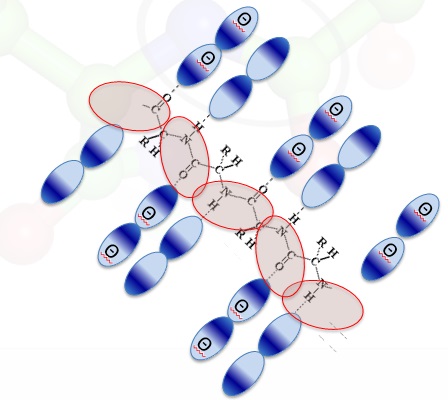
- первый слой связанной воды поляризует следующий и так в среднем до 6 молекул;
- вся вода в клетке связана (дополнительной поляризацией) и обладает характеристиками, отличными от обычной воды.
Магнитно-резонансная томография
Фамилии ученых и ссылки на их работы в книге Линга.
МРТ измеряет время вращательной корреляции атомов или протонов водорода в молекулах воды или время их релаксации (Т1 и Т2). Ограничение подвижности (фиксация) атомов водорода в молекулах воды в клетке приводит изменению времени Т1 и Т2 (по отношению к свободной воде), оно сокращается.
Вода в разных тканях отличается по временным параметрам Т1 и Т2. В злокачественных опухолях время Т1 и Т2 значительно больше, чем в клетках тканей, из которых опухоли произошли. Важно заметить, что дальнейшие опыты показали, что увеличение доли свободной воды – лишь одна из причин увеличения времени размагничивания атомов водорода (Т1 и Т2).
Роберт Дамадьян, создатель первого коммерческого МРТ-сканера благодарил в письме Линга за концепции биофизики воды, которые позволили ему создать первое МРТ-изображение тела человека.
Желатин и понимание коллоидов
56% полипептидной цепи желатина находится в полноразвернутой конформации и доступно воде.
В плане аминокислотного состава желатин на 13% состоит из пролина и на 10% из гидроксипролина, аминокислот, неспособных к образованию α-спиральных и β-складчатых структур в виду отсутствия атома водорода у их пирролидинового атома азота.
Также 33% аминокислотных остатков принадлежит «разрушителю спиралей» глицину. И в молекуле желатина нет дисульфитных мостиков (-S-S-), стабилизирующих третичную структуру.
С открытием теории многослойной организации поляризованной воды в клетке, можно дать новое определение коллоидам. «Коллоид – это кооперативный ансамбль полногразвернутых макромолекул (или их агрегатов) и полярного растворителя (например, воды). Макромолекулы формирующие коллоидную систему, характеризуются геометрически правильным чередованием диполей (групп NH и CO пептидной связи белков или диполей иной природы) или фиксированных зарядов вдоль полимерной цепи. При растворении такие макромолекулы взаимодействуют с полярным растворителем, ограничивая подвижность его молекул в результате многослойно адсорбции на своей поверхности, правильно расположенные заряды которой ориентируют их в пространстве и поляризуют. Поляризованность (увеличение дипольного момента молекул растворителя) – важнейшая предпосылка формирования многослойной структуры связанной воды.»
Коллоиды – экстравертная модель. Большинство глобулярных белков интвертны, большая часть их полипептидной цепи недоступна воде.
Новая гипотеза о коацервации
Коацервация – это расслоение гомогенного водного раствора на две несмешиваемые фазы с четкой границей между ними.
С точки зрения теории МОПВ коацервация – автокооперативный переход, во время которого одновременно протекает три процесса:
а) стягивание молекул воды вокруг поверхности полноразвернутой экстравертной молекулы, и их ориентация и поляризация полярными группами макромолекулы (каких, как CO и NH пептидных связей) с образованием многослойной структуры вдоль макромолекулы; затем водно-белковые комплексы сливаются в единый ассоциат, в котором все макромолекулы целиком включены в единый водный «кокон»;
б) вытеснение части избыточной воды ассоциата в фазу, бедную экстравернтым веществом, в результате оптимизации структуры ассоциата;
в) в формировании поверхности коацервата из линейных макромолекул (со связанной и структурированной водой), ориентированных перпендикулярно поверхности раздела фаз и образующих с такими же соседними макромолекулами непрерывную структурированную водную оболочку вокруг коацервата; таким образом формируется граница между богатой экстраверным веществом коацерватной фазой и бедной экстравертным веществом фазой растворителя, молекулы которого по степени упорядоченности не отличаются от обычной объемной воды; таким образом, граница раздела фаз – это граница раздела между двумя состояниями воды.
Причина, по которой процесс коацервации запускается при повышении температуры, состоит в вытеснении наименее поляризованных молекул воды из коцерватной фазы в среду в результате «стремления» поляризованных водных оболочек макромолеку к слиянию между собой, так как энергия взаимодействия поляризованных молекул воды между собой выше, чем «обычных» в силу более прочных водородных связей. В результате прирост энтропии системы коацерват-среда, связанный с выходом молекул воды из конденсированной фазы (так как доля структурированной в системе при этом снижается), начинает перевешивать вклад в термодинамику системы процесса слияния структурированных водных оболочек, снижающих энтропию и свободную энергию системы. Этот процесс термодинамически выгоден и приводит к дополнительной поляризации молекул связанной воды, и как следствие, – к утолщению водных слоев в пространстве в пространстве между макромолекулами. Рост энтропии системы, таким образом, является движущей силой коацервации.
Почему вышеназванная модель так важна:
1). Она объясняет резкую очерченность границ коацервата, а значит его способности не смешивать с окружающей водой. До Линга молекулярный механизм подобных явлений предложить не удавалось;
2). Модель объясняет почему только полноразвернутые белковые сети могут образовывать коацерваты, только они могут связывать воду в форме многослойной структуры поляризованных молекул, объем которой может быть значительным.
3). Она отвечает на вопрос почему протоплазма из поврежденных клеток – от инфузории Дюжардена до клеток Bryopsis Лепешкина – не смешивается с водой: она просто представляет собой коацерват.
Грубо говоря, Линг объяснил, что клетка – не водный раствор с «ништяками» в липидной оболочке, а что клетка – это белково-водно-[электролитная] (о последнем позже), структура которой удерживается за счет многослойной организации поляризованной воды вокруг полноразвернутых белковых структур. При том, что теория Линга на практике подтверждается, а теория липидных мембран противоречит данным наблюдений, так как клетка абсорбирует больше воды, чем может объяснить мембранная теория.
Количественная теория распределения веществ между клеточной водой и водой окружающей среды вследствие их вытеснения из клетки или модельных систем
Мы имеем простую физическую и экспериментально подтвержденную основу того, почему и за счет чего клетка вытесняет воду.
Соответственно, теория МОПВ может объяснить следующим образом низкую концентрацию Na+ и сахарозы в клетке по сравнению с равновесной внешней средой: энергия и энтропия.
Энергия. На образование «дыры» для иона Na+ (или молекулы сахарозы, или другого вещества) тратится больше энергии, чем выделяется при схлопывании таких «дыр» в обычной воде при переходе Na+ из среды в клетку. Это неравенство – основная энергетическая причина вытеснения растворенных веществ из клетки.
Энтропия (порядок). Сеть молекул структурированной воды ограничивает вращательные движения растворенных в ней молекул, поэтому их вращательная энтропия ниже в клетке, чем в среде. Поскольку вращательная энтропия составляет основную часть общей энтропии молекул вроде сахарозы и таких многоатомных образований, как гидратированные ионы Na+, уменьшение их энтропии в сочетании с энергозатратным «дырообразованием» в клетке делает растворение подобных веществ в клеточной воде термодинамически невыгодным.
Чем крупнее молекула вещества, тем больше сказывается влияние указанных термодинамических факторов, тем меньше их растворимость в клетке. Отсюда вытекает «правило размера»: истинный коэффициент равновесного распределения (q) вещества между клеточной водой (или водой, связанной экстравертной моделью) и внешней средой обратно пропорционален молекулярному объему вещества. Это было проверено в экспериментах, о которых можно почитать в книге Линга, где сравнивается распределение молекул с различным молярным объемом между мышечным волокном и средой.
Итоги
Основное положение заключается в многослойной организации поляризованной воды в клетке. См. предыдущую заметку.
Поляризующие структуры в мышечных волокнах (лягушки) отделены друг от друга в среднем 6 слоями воды. Это не мало, так как это вся клеточная вода. Таким образом в состоянии покоя свободной воды клетка в себе не содержит.
Напряжение вытеснения и поверхностный компонент энергии поляризации в любой точке клетки одинаковы.
Есть количественные методы определения избыточной энергии взаимодействия молекул связанной воды.
Теория МОПВ объясняет различие растворяющей способности среды и клетки. Превышение энергии взаимодействия молекул воды в адсорбирующих слоях по сравнению с объемной водой всего на 126 кал/моль способно привести к вытеснению из клеточной воды таких крупных ионов и молекул, как гидратированный ион натрия или молекула сахарозы. Простой, проверяемый и замечательный метод. Опыты с различными молекулами и клеткой / эстравертной лабораторной моделью смотрите в книге Линга.
P.S. Все простое закончилось. Дальше перейду к собственно теории ассоциации-индукции. И затем расскажу про незатронутую тут осмотическ